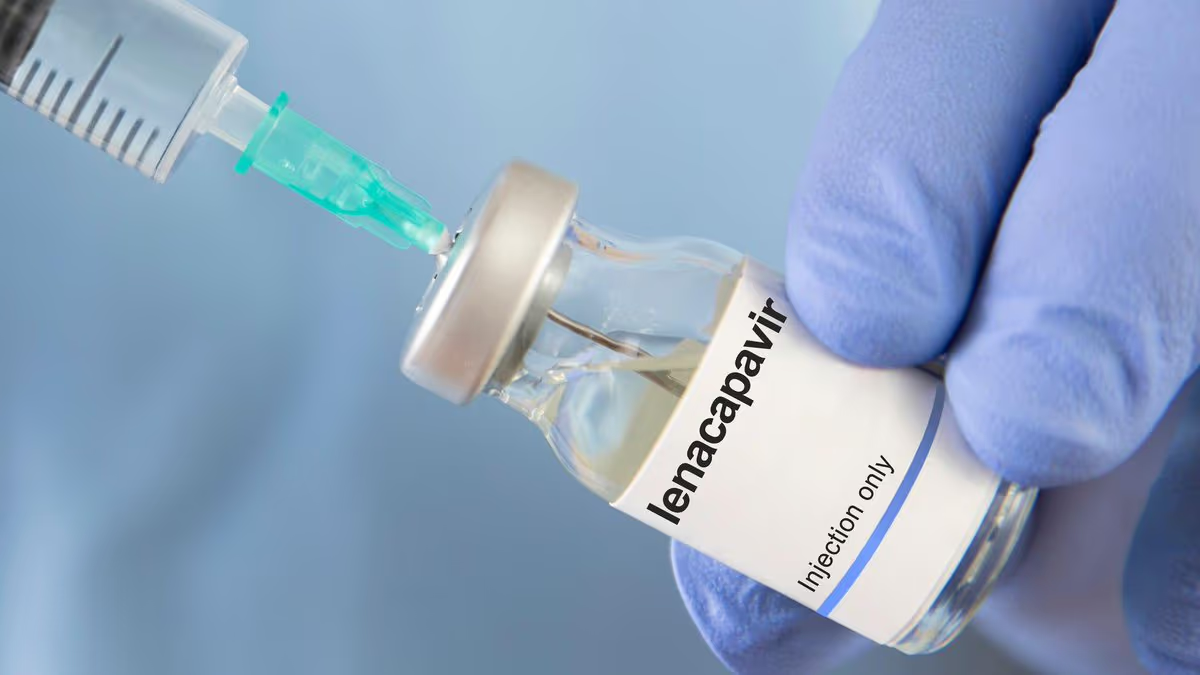
A Agência Nacional de Vigilância Sanitária (Anvisa) oficializou o registro do lenacapavir para a profilaxia pré-exposição (PrEP) ao HIV-1 por contato sexual. O medicamento poderá ser utilizado por adultos e adolescentes a partir de 12 anos, com peso mínimo de 35 quilos, desde que apresentem diagnóstico laboratorial negativo para o vírus. A autorização representa um avanço significativo nas estratégias de prevenção ao HIV no país.
O lenacapavir atua bloqueando diferentes etapas do funcionamento do capsídeo viral, impedindo a replicação do HIV no organismo. O esquema de uso prevê uma fase inicial com comprimidos orais, seguida por aplicações subcutâneas a cada seis meses. Estudos clínicos apontaram proteção completa em grupos de mulheres cisgênero e eficácia até 89% superior à profilaxia oral diária atualmente disponível, além de reduzir drasticamente falhas relacionadas à interrupção do tratamento.
A Organização Mundial da Saúde (OMS) passou a recomendar o lenacapavir como alternativa preventiva adicional em julho de 2025, classificando-o como a opção mais eficaz disponível após o desenvolvimento de vacinas. O medicamento já havia sido aprovado por autoridades regulatórias dos Estados Unidos e da União Europeia, reforçando sua credibilidade científica e segurança.
Apesar da liberação sanitária, a comercialização no Brasil ainda depende da definição do preço máximo pela Câmara de Regulação do Mercado de Medicamentos. Já a oferta gratuita pelo Sistema Único de Saúde (SUS) será avaliada pelo Ministério da Saúde, por meio da Comissão Nacional de Incorporação de Tecnologias. Além da prevenção, o lenacapavir também foi aprovado para o tratamento de pacientes com resistência a múltiplas terapias antirretrovirais, ampliando seu papel nas políticas de combate ao HIV no país.